Острый коронарный синдром (ОКС) — «рабочий диагноз», или термин, который базируется на клинических симптомах заболевания (боль в груди продолжительностью 20 минут и больше, что не прекращается после приёма нитроглицерина и сопровождается изменениями на ЕКГ). Этот термин появился из-за необходимости выбора тактики лечения до постановки окончательного диагноза.
- Что такое острый коронарный синдром и почему он возникает?
- Как происходит развитие ОКС?
- ДиагностикаИнструментальные методыОпределение биомаркеровСцинтиграфия миокардаКоронарная ангиография
- Инструментальные методы
- Определение биомаркеров
- Сцинтиграфия миокарда
- Коронарная ангиография
- Клиническое течение и стадии развития заболевания
- Лечение и оказание помощи
- Антитромботическая терапия
- Реабилитация и дальнейшее наблюдение пациента
- Выводы
Что такое острый коронарный синдром и почему он возникает?
Существуют определенные факторы риска, связанные с острым коронарным синдромом, о которых важно знать. К ним относятся:
- возраст – возраст – для мужчин 45 лет и старше, для женщин — 55 лет и больше;
- высокое артериальное давление;
- повышение уровня холестерина крови;
- курение;
- отсутствие физической активности;
- несоблюдение диеты, ожирение или избыточный вес;
- алкоголизм;
- диабет;
- наследственные факторы;
- стресс.
Но тем ни менее причиной ОКС №1 является атеросклероз – его обнаруживают у 70 – 95% пациентов.
Как происходит развитие ОКС?
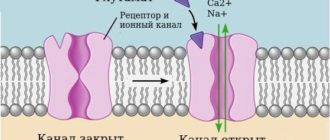
ОКС начинается, когда разрушенная атеросклеротическая бляшка стимулирует агрегацию тромбоцитов и образование кровяных сгустков в венечных артериях. В последующем этапе тромб закупоривает сосуд, уменьшая перфузию миокарда. Богатый на тромбоциты, он может выделять вазоконстрикторы — серотонин и тромбоксан А2. Это приводит к сужению просвета сосуда в месте разрыва атеросклеротической бляшки и к еще большей ишемии. Степень закупорки артерий, вызванная тромбом, определяет количество пораженного миокарда и тип ОКС:
- нестабильная стенокардия — частичная / прерывистая окклюзия, отсутствие повреждения миокарда;
- неQ-инфаркт — частичная / прерывистая окклюзия, повреждение миокарда;
- Q-инфаркт — полная окклюзия, повреждение миокарда.
Клетки миокарда требуют кислорода и аденозина 5b-трифосфата (АТФ) для поддержания сократимости и электрической стабильности. Поскольку они его лишены — происходит анаэробный метаболизм гликогена, образуется меньше ATФ, что приводит к сбою натриево-калиевых и кальциевых насосов и накоплению ионов водорода и лактата. В последующем всё это ведет к ацидозу. Если перфузию миокарда не восстановить в течение примерно 20 минут, наступают необратимые повреждения, приводящие к некрозу.
Диагностика
В первую очередь диагностика ОКС начинается со сбора анамнеза и детализации жалоб: продолжительная (больше 20мин. ) интенсивная боль в груди давящего характера, одышка, страх смерти — аналогичный симптомокомплекс практически не встречается при других патологиях сердца. Основной целью физикального обследования является исключение болей некардиального генеза, неишемических заболеваний сердца, а также любых патологий, потенциально способствующих усилению ишемии.
Инструментальные методы
Электрокардиограмма (ЭКГ) в покое – является «золотым методом» диагностики ОКС, а также скрининговым методом для других заболеваний, сопровождающихся болевым синдромом. ЭКГ в покое необходимо сравнивать с предварительной кардиограмой и с ЭКГ после исчезновения болей. Еще одним преимуществом этого метода является простота исполнения — ведение пациентов доступно и в стационаре, и в поликлинике, и в амбулатории семейного типа.
Определение биомаркеров
Во время ИМ происходит отмирание клеток сердца. Ферменты из кардиомиоцитов попадают в кровяное русло и некоторое время продолжают циркулировать в нём. С помощью специальных анализов можно определить концентрацию этих веществ, оценить степень повреждения, а также установить сам факт некротических изменений в сердечной мышце.
Маркерами некротических изменений в миокарде являются:
- Тропонин-Т.
- Тропонин-I.
- Миоглобин.
- Креатинфосфокиназа (МВ).
ЭхоКГ — этот метод широко используется для уточнения диагноза, но не подходит для его постановки, так как не позволяет увидеть маленькие очаги некроза.
Признаками ОКС являются:
- Патологическая работа клапанов.
- Увеличение камер сердца.
- Турбулентный поток крови.
- Расширенная нижняя полая вена.
Сцинтиграфия миокарда
Этот метод используют при необходимости определения точной локализации некротического очага. Суть его состоит в том, что здоровые и повреждённые клетки имеют разную биохимическую активность. При введении специальных реактивов, последние будут накапливаться избирательно либо в здоровых, либо в мертвых клетках (зависит от реактива), что позволит точно определить наличие повреждённых областей.
Коронарная ангиография
Коронарография является достаточно сложным, но достаточно информативным методом исследования ОКС. Его суть – выполнение рентгенографического снимка после введения в венечные артерии контрастного вещества. Коронарография позволяет определить точное место и степень сужения пораженной артерии.
Обязательными (стандартными) диагностическими мероприятиями при подозрении на ОКС являются электрокардиограмма и определение маркеров некроза. Остальные назначаются при необходимости — в зависимости от специфики болезни у каждого пациента.
Клиническое течение и стадии развития заболевания
Классификация острого коронарного синдрома позволяет разделить больных на две группы:
- Больные с болью в груди, продолжительностью более 20 мин., которая не снимается приемом нитроглицерина. На ЕКГ — элевация сегмента ST, что свидетельствует об острой окклюзии коронарной артерии. В дальнейшем это приводит к возникновению Q-инфаркта.
- Больные с болью в груди, продолжительностью более 20 мин., которая не снимается приемом нитроглицерина и пациенты с впервые возникнувшей стенокардией III класса без устойчивого подъема сегмента ST (депрессия, изменение T). Такое состояние трансформируется в не-Q-инфаркт или в нестабильную стенокардию.
Лечение и оказание помощи
Неотложная помощь при остром коронарном синдроме зависит от его варианта и проводится на основании специально разработанных протоколов. При ОКС с элевацией сегмента ST:
- Пациентам, госпитализированным не позднее 12 часов после появления симптомов показана механическая (чрескожное коронарное вмешательство (ЧКВ) или фармакологическая реперфузия).
- Предпочтение отдается ЧКВ, если его производят не позднее 120мин. После первого обращения за медицинской помощью.
- При невозможности выполнения ЧКВ на протяжении 120мин. Производят тромболизисную терапию.
- В случае успешного тромболизиса больного направляют в центр для проведения коронарной ангиографии на протяжении 3-24час. При неэффективном тромболизисе необходима срочная ангиография.
- Антитромбоцитарная и антикоагулянтная терапия.
- Гиполипидемическая терапия.
Алгоритм помощи при ОКС без элэвации сегмента ST:
- Оценка клинического состояния, подтверждение диагноза.
- Медикаментозная терапия: антиишемические средства, антикоагулянты и антиагреганты.
- Коронарная реваскуляризация.
- Статины.
Нитроглицерин представляет собой сосудорасширяющее средство, которое снижает потребность миокарда в кислороде. Его вводят сублингвально или с помощью буккального спрея (0,3-0,6 мг) каждые 5 минут, в общей сложности 3 дозы. Если боль сохраняется, следует начать введение внутривенного нитроглицерина (начальная скорость 5-10 мкг/мин с её увеличением до 10 мкг/мин каждые 3 — 5 минут до ослабления симптомов). Абсолютными противопоказанием к применению нитроглицерина является гипотензия.
Морфин и другие анальгетики
Морфин рекомендуется после 3 доз нитроглицерина, или когда симптомы ишемии повторяются во время лечения. В таких случаях от 1 до 5 мг морфина сульфата можно вводить внутривенно каждые 5-30 минут при необходимости, с тщательным контролем артериального давления и частоты дыхания. Морфин действует как мощный анальгетик.
β- блокаторы ингибируют β-1 адренергические рецепторы в миокарде, уменьшают его сократимость и сердечный ритм. При отсутствии противопоказаний, терапия пероральными формами β-блокаторов должна быть начата в течение первых 24 часа. Для всех пациентов доза препарата должна быть скорректирована для достижения частоты сердечных сокращений от 50 до 60 ударов в минуту.
Ингибиторы системы Ренин-Ангиотензин-Альдостерон
В зарубежных рекомендациях отмечено, что при отсутствии гипотензии или других известных противопоказаний пероральное введение ингибитора ангиотензинпревращающего фермента (эналаприл, лизиноприл) или блокатора рецептора ангиотензина II, для пациентов, которые не переносят ингибиторы АПФ (валсартан,лозартан) в течение первых 24 часов позволило существенно снизить количество летальных исходов.
Антитромботическая терапия
Антитромботическая терапия является краеугольным камнем лечения пациентов с ОКС. Она включает два компонента: антитромбоцитарную и антикоагулянтную терапию.
Аспирин. Он блокирует синтез тромбоксана А2 путем необратимого ингибирования циклооксигеназы-1, тем самым уменьшая агрегацию тромбоцитов. Первоначальная суточная доза должна становить от 162 до 325 мг, а затем уменьшается — от 75 до 162 мг. Используется для долгосрочной вторичной профилактики.
Клопидогрель является рекомендуемой альтернативой для пациентов, которые не переносят аспирин. Он уменьшает активацию и агрегацию тромбоцитов и снижает вязкость крови. Нагрузочная доза составляет 600 мг, поддерживающая – 75мг на день. Терапия клопидогрелем и аспирином рекомендуется практически всем пациентам с ОКС.
Антикоагулянтная терапия должна начинаться как можно скорее после постановления диагноза. На сегодняшний день для её проведения используют такие препараты: нефракционированный гепарин, эноксапарин, фондопаринукс.
Нефракционированный гепарин(НФГ). Результаты нескольких рандомизированных исследований свидетельствуют о том, что прием НФГ ассоциируется с более низкими показателями смертности нежели терапия исключительно аспирином. Но при его назначении необходимо наблюдение за активированным частичным тромбопластиновым временем (ЧТВ) для предотвращения кровоизлияний.
Фондопаринукс — синтетический пентасахарид, который является непрямым ингибитором фактора Ха и требует антитромбина для достижения терапевтического эффекта. Этот препарат предпочтительнее других антикоагулянтов для пациентов, которым проводится консервативная терапия и у пациентов с повышенным риском кровотечения.
В отсутствие противопоказаний, липидопонижающая терапия со статинами должна быть начата для всех пациентов с ОКС, независимо от базового уровня холестерина и ЛПНП.
Проводится на догоспитальном этапе. Если это невозможно — не позднее 30 минут после госпитализации. Используют препараты следующих видов:
- Стрептокиназа – 1,5 млн., ОД в/в на протяжении 30-60мин;
- Альтеплаза — 15мг в/в болюсно, 0,75 мг/кг массы тела на протяжении 30мин, дальше по 0,5 мг/кг на протяжении 60мин.; общая доза не должна превышать 100мг;
- Тенектоплаза – болюсное в/в введение препарата зависит от массы больного: 30 мг при массе меньше 60 кг; 35 мг на 60-69кг; 40мг на 70-79кг; 45мг на 80-89кг; 50мг на массу больше 90кг.
Операции для лечения ОКС
Хирургическое лечение острого коронарного синдрома направлено на восстановление кровообращения в венечных артериях. Позволяют этого достичь аортокоронарное шунтирование и стентирование. Суть первого метода лежит в создании обходного пути для артериальной крови, избегая пораженного участка. Таким образом, те участки сердца, которые страдали от гипоксии, начинают снова нормально функционировать. Суть стентирования заключается в постановке в артерию стента, который расширит ссуженный участок и будет препятствовать дальнейшему росту бляшки.
Реабилитация и дальнейшее наблюдение пациента
Реабилитация сердца включает в себя:
- диетическое консультирование;
- назначение комплекса упражнений;
- психосоциальную поддержку;
- отказ от курения;
Целью является быстрое и полное восстановление организма и снижение вероятности повторения ОКС. Программа реабилитации фокусируется на улучшении физического состояния, уверенности в себе и социальной интеграции. Она проводится с помощью врача, специализированных физиотерапевтов, медсестер и подразделяется на госпитальный и поликлинический этапы. Кроме того, необходимы постоянные консультации у лечащего доктора.
Выводы
За прошедшую четверть века были достигнуты колоссальные успехи в нашем понимании патофизиологии ОКС, и эти достижения сопровождались огромные прорывами в управлении этим состоянием. Точная диагностика острого коронарного синдрома имеет жизненно важные последствия и требует тщательной оценки анамнеза пациента, результатов физического обследования, ЭКГ с 12 отведениями и анализа биомаркеров сердца. Руководство по лечению ОКС включает как агрессивную медицинскую терапию, так и реваскуляризацию. А раннее выявление симптомов и своевременная профилактика этого заболевания позволят избежать негативных последствий и сберечь здоровье на многие годы.
ВВЕДЕНИЕ
В конце 2019 г. в Китайской Народной Республике (КНР) произошла вспышка
новой коронавирусной инфекции с эпицентром в городе Ухань (провинция
Хубэй). Всемирная организация здравоохранения (ВОЗ) 11 февраля 2020 г. определила официальное название инфекции, вызванной новым коронавирусом,
– COVID-19 («Coronavirus disease 2019»). Международный комитет по
таксономии вирусов 11 февраля 2020 г. присвоил официальное название
возбудителю инфекции – SARS-CoV-2.
Появление COVID-19 поставило перед специалистами здравоохранения задачи,
связанные с быстрой диагностикой и оказанием медицинской помощи больным. В настоящее время продолжается интенсивное изучение клинических и
эпидемиологических особенностей заболевания, разработка новых средств
его профилактики и лечения. Наиболее распространенным клиническим
проявлением
нового варианта коронавирусной инфекции является двусторонняя пневмония
(вирусное диффузное альвеолярное повреждение с микроангиопатией), у 3-4%
пациентов зарегистрировано развитие острого респираторного
дистресс-синдрома (ОРДС). У части больных развивается
гиперкоагуляционный синдром с тромбозами и тромбоэмболиями, поражаются
также другие органы и системы (центральная нервная система, миокард,
почки, печень, желудочно-кишечный тракт, эндокринная и иммунная
системы), возможно развитие сепсиса и септического шока.
Рекомендации, представленные в документе, в значительной степени
базируются на материалах по диагностике, профилактике и лечению
COVID-19, опубликованных специалистами ВОЗ, китайского, американского и
европейского центров по контролю за заболеваемостью, анализе
отечественных и зарубежных научных публикаций, нормативно-правовых
документах Правительства Российской Федерации, Минздрава России и
Роспотребнадзора.
Мероприятия по предупреждению завоза и снижению рисков распространения
COVID-19 на территории Российской Федерации регламентированы
распоряжениями Правительства Российской Федерации от 30. 2020 № 140-р,
от 31. 2020 № 154-р, от 03. 2020 № 194-р, от 18. 2020 № 338-р, от
27. 2020 № 447-р, от 27. 2020
№ 446-р, от 27. 2020 № 448-р от 16. 2020 № 635-р, от 06. 2020 №
550-р, от 12. 2020 № 597-р, от 14. 2020 № 622-р, от 16. 2020 №
730-р, от 27. 2020
№ 763-р, от 01. 2020 № 1996-р, от 01. 2020 № 1997-р, от 02. 2020
№2236-р, от 12. 2020 № 2338-р, от 20. 2020 №2406-р, от 14. 2020
№2649-р
и постановлениями Главного государственного санитарного врача Российской
Федерации от 24. 2020 № 2, от 31. 2020 № 3, от 02. 2020 № 5, от
13. 2020 № 6,
от 18. 2020 № 7, от 30. 2020 № 9, от 03. 2020 № 10, от 13. 2020
№ 11,
от 22. 2020 № 15, от 07. 2020 г. № 18, от 13. 2020 № 20, от
15. 2020 № 21,
от 27. 2020 № 22, от 18. 2020 № 27, от 16. 2020 № 31, от
13. 2020 № 34,
от 13. 2020 № 35, от 21. 2020 № 43, от 09. 2021 № 12, от
16. 2021 № 13.
Мероприятия по недопущению распространения COVID-19 в медицинских
организациях проводятся в соответствии с приказом Минздрава России от
19. 2020
№ 198н «О временном порядке организации работы медицинских организаций в
целях реализации мер по профилактике и снижению рисков распространения
новой коронавирусной инфекции COVID-19» (в ред. приказов Минздрава
России от 27. 2020 № 246н, от 02. 2020 № 264н, от 29. 2020 № 385н,
от 18. 2020
№ 459н, от 29. 2020 № 513н, от 07. 2020 № 685н, от 27. 2020 N
905н, от 15. 2020 № 982н, от 01. 2020 № 1062н, от 23. 2020 №
1140н, от 30. 2020
№1184н, от 04. 2020 № 1288н, от 23. 2021 № 232н).
Методические рекомендации предназначены для руководителей медицинских
организаций и их структурных подразделений, врачей-терапевтов, врачей
общей практики, врачей-инфекционистов, врачей-педиатров,
врачей-акушеров-гинекологов, врачей-реаниматологов отделений интенсивной
терапии инфекционных стационаров, врачей скорой медицинской помощи, а
также иных специалистов, работающих в сфере лабораторной и
инструментальной диагностики и организации оказания медицинской помощи
пациентам с COVID-19.
ЭТИОЛОГИЯ, ПАТОГЕНЕЗ И ПАТОМОРФОЛОГИЯ
Коронавирусы (Coronaviridae) – это большое семейство РНК-содержащих
вирусов, способных инфицировать как животных (их естественных хозяев),
так и человека. По результатам серологического и филогенетического
анализа коронавирусы разделяются на четыре рода: Alphacoronavirus,
Betacoronavirus, Gammacoronavirus и Deltacoronavirus. У людей
коронавирусы могут вызвать целый ряд заболеваний – от легких форм острой
респираторной инфекции (ОРВИ) до тяжелого острого респираторного
синдрома (ТОРС или SARS). В настоящее время среди населения циркулируют
четыре сезонных коронавируса (HCoV-229E, -OC43, -NL63 и -HKU1), которые
круглогодично присутствуют в структуре ОРВИ, и, как правило, вызывают
поражение верхних дыхательных путей легкой и средней степени тяжести, а
также два высокопатогенных коронавируса – вирус ближневосточного
респираторного синдрома (MERS) и новой коронавирусной инфекции COVID-19.
До 2002 г. коронавирусы рассматривались в качестве агентов, вызывающих
нетяжелые заболевания верхних дыхательных путей (с крайне редкими
летальными исходами). В период с 2002 по 2004 гг. коронавирус SARS-CoV
из рода Betacoronavirus (резервуар – летучие мыши, промежуточный
резервуар – циветты) впервые стал причиной развития эпидемии так
называемой атипичной пневмонии (ТОРС) и подтвержденной причиной смерти
774 человек в 37 странах мира. С 2004 г. новых случаев атипичной
пневмонии, вызванной SARS-CoV, не зарегистрировано. Очередная
эпидемия, вызванная коронавирусом MERS-CoV (резервуар – одногорбые
верблюды), также из рода Betacoronavirus – ближневосточный
коронавирусный синдром, началась в 2012 г. на Аравийским полуострове
(82% случаев в Саудовской Аравии). До 2020 г. зарегистрировано 866
летальных исходов от MERS. В настоящий момент MERS-CoV продолжает
циркулировать и вызывать новые случаи заболевания.
SARS-CoV-2 – вирус с одноцепочечной РНК позитивной полярности,
относящийся к семейству Coronaviridae, роду Betacoronavirus. Генетическая последовательность SARSCoV-2 сходна с последовательностью
SARS-CoV по меньшей мере на 79%. Генетический анализ свыше 200 тысяч
геномов SARS-CoV-2, полученных в результате секвенирования, позволяет
выделить отдельные генетические группы возбудителя, часто связанные с
его циркуляцией в определенных географических областях мира.
Появление мутаций является типичным для РНК-содержащих вирусов. Анализ
различных линий циркулирующих штаммов SARS-CoV-2 в начале мая 2020 года
показал, что их разнообразие внутри отдельных стран постепенно
снижается, вероятно, из-за исчезновения некоторых вирусных линий и
быстрого распространения других (доминирующих) линий. Исходный штамм,
выделенный из образцов от пациентов, госпитализированных в Ухане в
декабре 2019 года, был отнесен к генетическому клайду L и является
референсным геномом для всех последующих полученных при секвенировании
последовательностей. В начале января 2020 года несколько изменившийся
штамм SARS-CoV-2 был отнесен к клайду S, а затем также выделили клайд О.
Первоначальное разделение вирусов SARS-CoV-2 на клайды базировалось на
минорных мутациях в структуре генома, которые не имели значения для
практического здравоохранения, поскольку не изменяли биологические
свойства вируса (вирулентность, контагиозность, чувствительность к
противовирусным препаратам). В дальнейшем, циркулирующие штаммы
SARS-CoV-2 также продолжали накапливать отдельные точечные мутации в
геноме, которые привели к выделению следующих двух клайдов: клайда V в
середине января 2020 года (с мутациями в белках NSP6 и ORF3) и клайда G
с характерной мутацией D614G. Данный клайд также разделился впоследствии
(примерно с февраля 2020 года) на два подклайда GR и GH, самые
распространенные в мире. Большинство выделенных в России вирусов также
относятся к клайду G (GR и GH).
В декабре 2020 г. в Великобритании выявлен новый вариант возбудителя —
VUI 202012/01 (вариант в стадии расследования, 2020 год, месяц 12,
вариант 01). Исследования свойств VUI 202012/01 продолжаются. Однако к
настоящему времени не сообщалось о более тяжелом течении или более
высокой летальности при инфекции, вызванной новым вариантом. Большинство
зарегистрированных мутаций SARS-CoV-2
не имеют функционального значения. В настоящее время нет данных о связи
мутаций в геноме SARS-CoV-2 с тяжестью и прогнозом течения COVID-19.
Учитывая высокую патогенность, вирусы SARS-CoV, SARS-CoV-2 и MERS-CoV
отнесены ко II группе патогенности.
При комнатной температуре (20-25 °С) SARS-CoV-2 способен сохранять
жизнеспособность на различных объектах окружающей среды в высушенном
виде до 3 суток, в жидкой среде – до 7 суток. Вирус остается стабильным
в широком диапазоне значений рН (до 6 дней при значении рН от 5 до 9 и
до 2 дней при рН4 и рН11). При температуре +4 °С стабильность вируса
сохраняется более 14 дней. При нагревании до 37 °С полная инактивация
вируса происходит в течение 1 дня, при 56 °С — в течение 45 минут, при
70 °С – в течение 5 минут. Вирус чувствителен к ультрафиолетовому
облучению дозой не менее 25 мДж/см2 и действию различных
дезинфицирующих средств в рабочей концентрации.
Входные ворота возбудителя – эпителий верхних дыхательных путей и
эпителиоциты желудка и кишечника. Начальным этапом заражения является
проникновение SARS-CoV-2 в клетки-мишени, имеющие рецепторы
ангиотензинпревращающего фермента II типа (АПФ2). Клеточная
трансмембранная сериновая протеаза типа 2 (ТСП2) способствует связыванию
вируса с АПФ2, активируя его S-протеин, необходимый для проникновения
SARS‑CoV‑2 в клетку. В соответствии с современными представлениями АПФ2
и ТСП2 экспрессированы на поверхности различных клеток органов дыхания,
пищевода, кишечника, сердца, надпочечников, мочевого пузыря, головного
мозга (гипоталамуса) и гипофиза, а также эндотелия и макрофагов.
Нуклеокапсидный белок вируса был обнаружен в цитоплазме эпителиальных
клеток слюнных желез, желудка, двенадцатиперстной и прямой кишки,
мочевыводящих путей, а также в слезной жидкости. Однако основной и
быстро достижимой мишенью SARS-CoV-2 являются альвеолярные клетки II
типа (AT2) легких, что определяет развитие диффузного альвеолярного
повреждения. Полагают, что при COVID-19 может развиваться катаральный
гастроэнтероколит, так как вирус поражает клетки эпителия желудка,
тонкой и толстой кишки, имеющие рецепторы АПФ2. Однако его
морфологические особенности изучены недостаточно. Есть данные о
специфическом поражении сосудов (эндотелия), а также миокарда, почек и
других органов. Изменения иммунокомпетентных органов изучены
недостаточно, обсуждается возможность специфического поражения
лимфоцитов с их апоптозом и пироптозом (лежит в основе характерной и
прогностически неблагоприятной лимфопении), синдрома гиперактивности
макрофагов и гемофагоцитраного синдрома, нетоза нейтрофильных лейкоцитов
(как одной из причин синдрома диссеминированного внутрисосудистого
свертывания (ДВС)).
На основании способности SARS-CoV-2 поражать различные органы и ткани
высказывается идея о существовании дополнительных рецепторов и
ко-рецепторов вируса помимо АПФ2. В частности, обсуждается роль CD147 в
инвазии клеток SARS‑CoV‑2.
Установлено, что диссеминация SARS-CoV-2 из системного кровотока или
через пластинку решетчатой кости может привести к поражению головного
мозга. Изменение обоняния (аносмия) у больных на ранней стадии
заболевания может свидетельствовать как о поражении ЦНС вирусом,
проникающим через обонятельный нерв, так и о морфологически
продемонстрированном вирусном поражении клеток слизистой оболочки носа,
не исключена роль васкулита.
При патологоанатомическом исследовании ткани легкого специфические
макроскопические признаки COVID-19 не установлены, хотя морфологическая
картина может рассматриваться как характерная. В наблюдениях, в которых
резко преобладают признаки тяжелой дыхательной недостаточности,
отмечается картина ОРДС («шокового легкого» или диффузного альвеолярного
повреждения): резкое полнокровие и диффузное уплотнение легких,
практически неотличимое от наблюдавшегося при «свином» гриппе А/H1N1pdm
(в 2009 г. и в последующие годы), кроме типичных для SARS‑CoV‑2
поражения сосудистой системы легких (эндотелиит) и выраженного
альвеолярно-геморрагического синдрома. Легкие увеличены в объеме и
массе, тестоватой или плотной консистенции, маловоздушные или
безвоздушные; лакового вида с поверхности, темно-красного (вишневого)
цвета, при надавливании с поверхностей разрезов стекает темно-красная
жидкость, с трудом выдавливаемая из ткани. Кроме разной величины
кровоизлияний, встречаются геморрагические инфаркты, обтурирующие
тромбы, преимущественно в ветвях легочных вен. Значимых поражений трахеи
при этом не наблюдается, выявляемый серозно-гнойный экссудат и гиперемия
слизистой оболочки у интубированных пациентов связаны с нозокомиальной
инфекцией. В случаях, когда COVID-19 присоединялся к другой тяжелой
патологии, закономерно отмечается сочетание изменений характерных для
разных заболеваний.
Характер морфологических изменений при легком течении COVID-19
неизвестен. Исходя из анализа клинической симптоматики, можно
предполагать тропность вируса к эпителию гортани, мерцательному эпителию
дыхательных путей на всем протяжении, альвеолоцитам I и II типов. Судя
по всему, вирусные поражения у таких пациентов не приводят к развитию
выраженного экссудативного воспаления и соответственно катаральных
явлений.
Критическая форма COVID-19 является разновидностью цитокинового шторма,
а ее проявления сходны с течением первичного и вторичного
гемофагоцитарного лимфогистиоцитоза (ГЛГ) или синдрома активации
макрофагов (САМ). При критическом течении COVID-19 развивается
патологическая активация врожденного
и приобретенного (Th1- и Th17-типы) иммунитета, «дисрегуляция» синтеза
«провоспалительных», иммунорегуляторных, «антивоспалительных» цитокинов
и хемокинов: ИЛ1, ИЛ2, ИЛ6, ИЛ7, ИЛ8, ИЛ9, ИЛ10, ИЛ12, ИЛ17, ИЛ18,
гранулоцитарный колониестимулирующий фактор (Г-КСФ), гранулоцитарно-
макрофагальный колониестимулирующий фактор (ГМ-КСФ), фактор некроза
опухоли α (ФНОα), ИФНγ-индуцируемый белок 10, ИФНα и ИФНβ, моноцитарный
хемоаттрактантный белок 1 (МХБ1), макрофагальный воспалительный белок 1α
(МВБ1α), а также маркеров воспаления (СРБ, ферритин).
Отличие COVID-19-индуцированного вторичного ГЛГ от других форм вирус-
индуцированного цитокинового шторма заключается в том, что
органом-мишенью при этом варианте цитокинового шторма являются легкие,
что связано с тропизмом коронавируса к легочной ткани, а также в более
умеренном повышении уровня ферритина сыворотки крови. Гиперактивация
иммунного ответа при COVID-19 часто ограничивается легочной паренхимой,
прилегающей бронхиальной и альвеолярной лимфоидной тканью, и
ассоциируется с развитием ОРДС.
В раннем периоде COVID-19-пневмонии наблюдаются нормальный уровень
фибриногена крови, регионального фибринолиза и высокий уровень D-димера,
что не является признаком развития острого синдрома активации
макрофагов. Этот процесс можно расценивать как САМ-подобное
внутрилегочное воспаление, которое усиливает выраженность локальной
сосудистой дисфункции, включающую микротромбоз и геморрагии, что в
большей степени приводит развитию легочной внутрисосудистой
коагулопатии, чем диссеминированного внутрисосудистого свертывания.
У пациентов с критическим течением COVID-19 развивается васкулярная
эндотелиальная дисфункция, коагулопатия, тромбозы с наличием антител к
фосфолипидам, с клинической картиной, напоминающей катастрофический
антифосфолипидный синдром. Клинические и патологические изменения трудно
дифференцировать с полиорганным тромбозом, развивающимся при ДВС и
тромботической микроангиопатии (ТМА).
Цитокиновый шторм при COVID-19, как правило, приводит к развитию ОРДС,
полиорганной недостаточности и может быть причиной летального исхода.
При микроскопическом исследовании обращают внимание интраальвеолярный
отек с примесью в отечной жидкости эритроцитов, макрофагов, слущенных
альвеоцитов, единичных нейтрофилов, лимфоцитов и плазмоцитов;
интраальвеолярные гиалиновые мембраны, распространяющиеся иногда до
внутренней поверхности бронхиол; десквамация альвеолярного (в виде
отдельных клеток и их пластов) и бронхиолярного эпителия; появление
крупных, неправильной формы альвеоцитов II типа, с увеличенными ядрами с
грубозернистым хроматином и отчетливыми ядрышками (в некоторых из них
вокруг ядра видно гало,
а в цитоплазме – округлые базофильные и эозинофильные включения,
характерные для вирусного повреждения клеток); пролиферация
альвеолоцитов II типа, образование их симпластов. Характерна слабо
выраженная периваскулярная и перибронхиальная лимфоидная и
макрофагальная инфильтрация, а также инфильтрация межальвеолярных
перегородок и стенок мелких сосудов, представленная различными
популяциями лимфоцитов и макрофагов. Преобладают CD3+ Т лимфоциты, среди
них – CD2+, CD5+, CD8+ Т-клетки. B-лимфоциты (CD20+, C80+) сравнительно
немногочисленны, натуральные киллеры (CD16+/CD56+) практически
отсутствуют. Вирус SARS-CoV-2 выявляется в реснитчатых клетках бронхов,
эпителии бронхиол, в альвеолоцитах и макрофагах, а также в эндотелии
сосудов с помощью методов амплификации нуклеиновых кислот (МАНК), при
иммуногистохимическом, ультраструктурном исследованиях.
Специфическое вирусное и вызванное цитокиновым штормом (а в более
поздние сроки – возможно и аутоиммунное) повреждение эндотелия,
получившее название SARS‑CoV‑2-ассоциированый эндотелиит, – основа
характерной для COVID-19 микроангиопатии преимущественно легких, реже –
других органов (миокарда, головного мозга и др. ), причем в ряде
наблюдений развивается локальный легочный или системный
продуктивно-деструктивный тромбоваскулит.
Изучается возможная связь между дефицитом фолиевой кислоты,
гипергомоцистеинемией и развитием осложнений COVID-19 со стороны
сердечно- сосудистой системы, а также значение их коррекции препаратами,
содержащими фолиевую кислоту, в лечении новой короновирусной инфекции.
В патогенезе COVID-19 поражение микроциркуляторного русла играет
важнейшую роль. Для поражения легких при COVID-19 характерны выраженное
полнокровие капилляров межальвеолярных перегородок, а также ветвей
легочных артерий и вен, со сладжами эритроцитов, свежими фибриновыми и
организующимися тромбами; внутрибронхиальные, внутрибронхиолярные и
интраальвеолярные кровоизлияния, являющиеся субстратом для
кровохарканья, а также периваскулярные кровоизлияния. Выраженный
альвеолярно-геморрагический синдром характерен для большинства
наблюдений, вплоть до формирования, фактически, геморрагических
инфарктов (хотя и истинные геморрагические инфаркты не редки). Тромбы
сосудов легких важно отличать от тромбоэмболов, так как тромбоэмболия
легочной артерии (ТЭЛА) также характерна для COVID-19. Тромбоз легочных
артерий иногда прогрессирует до правых отделов сердца, описан тромбоз
артерий разных органов с развитием их инфарктов (миокарда, головного
мозга, кишечника, почек, селезенки), описана также гангрена конечностей. Это отличает изменения в легких при COVID-19 от ранее наблюдавшихся при
гриппе A/H1N1 и других коронавирусных инфекциях. Несмотря на выраженный
альвеолярно-геморрагический синдром, значительных отложений гемосидерина
не наблюдается. Описанные поражения легких и других
органов являются причиной смерти без присоединения бактериальной или
микотической суперинфекции. Ее частота не превышает 30-35%, в основном у
больных при длительной искусственной вентиляции легких (ИВЛ).
В части наблюдений выявлены изменения и в других органах (помимо
васкулита), которые можно предположительно связать с генерализацией
коронавирусной инфекции: кишечнике (катаральный и геморрагический
гастроэнтероколит), головном мозге и мягкой мозговой оболочке (энцефалит
и менингит), сердце (миокардит), поджелудочной железе, почках,
селезенке. Весьма вероятны и прямые вирусные поражения плаценты, в
единичных наблюдениях показана возможность внутриутробного
инфицирования, клиническое значение которого требует дальнейшего
изучения. Отмечены тяжелые поражения микроциркуляторного русла в связи с
развитием ДВС, которые оказались наиболее выраженными в легких и почках. Описаны типичные для COVID-19 кожные проявления – от геморрагического
синдрома до высыпаний различного вида, патогенез которых не ясен. Есть
данные, что SARS‑CoV2 способен активировать предшествующие хронические
инфекционные процессы.
На основании исследований аутопсийного материала с учетом клинической
картины заболевания можно выделить, как минимум, следующие клинические и
морфологические маски COVID-19: сердечную, мозговую, кишечную, почечную,
печеночную, диабетическую, тромбоэмболическую (при тромбоэмболии
легочной артерии), септическую (при отсутствии бактериального или
микотического сепсиса), микроангиопатическую (с системной
микроангиопатией), кожную.
Таким образом, как и при других коронавирусных инфекциях, а также гриппе
А/H1N1 в большинстве наблюдений основным морфологическим субстратом
COVID-19 является диффузное альвеолярное повреждение, но, в отличие от
них, с одновременным тяжелым поражением сосудистого русла и у ряда
больных различных органов и систем. Термин вирусной (интерстициальной)
пневмонии, широко используемый в клинике, по сути своей отражает именно
развитие диффузного альвеолярного повреждения. В свою очередь, тяжелое
диффузное альвеолярное повреждение является синонимом клинического
понятия «острый респираторный дисстресс-синдром» (ОРДС).
Многие аспекты патогенеза и патоморфологии коронавирусной инфекции
нуждаются в дальнейшем комплексном изучении с использованием современных
методов.
ЭПИДЕМИОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА
С декабря 2019 г. по март 2020 г. наиболее широкое распространение
SARS-CoV-2 получил на территории КНР, в которой подтвержденные случаи
заболевания были зарегистрированы во всех административных образованиях.
Наибольшее количество заболевших выявлено в Юго-Восточной части КНР с
эпицентром в провинции Хубэй (84% от общего числа случаев в КНР).
С конца января 2020 г. во многих странах мира стали регистрироваться
случаи COVID-19, преимущественно связанные с поездками в КНР. В конце
февраля 2020 г. резко осложнилась эпидемиологическая обстановка по
COVID-19 в Южной Корее, Иране и Италии, что в последующем привело к
значительному росту числа случаев заболевания в других странах мира,
связанных с поездками в эти страны. ВОЗ объявила 11 марта 2020 г. о
начале пандемии COVID-19.
Почти все страны мира серьезно пострадали от пандемии COVID-19, однако
эпидемическая ситуация в разных странах крайне неоднородная. Высокий
уровень заболеваемости и летальности отмечается в тех странах, где
изоляционно- ограничительные мероприятия были введены с запозданием или
в неполном объеме (Италия, Испания, США, Великобритания). Напротив, в
странах, в которых противоэпидемические мероприятия были введены
своевременно и в полном объеме (Сингапур, Южная Корея, Тайвань, Япония),
наблюдается низкий уровень заболеваемости и летальности от COVID-19.
Источником инфекции является больной человек, в том числе находящийся в
инкубационном периоде заболевания, и бессимптомный носитель SARS-CoV-2. Наибольшую опасность для окружающих представляет больной человек в
последние два дня инкубационного периода и первые дни болезни.
Передача инфекции осуществляется воздушно-капельным, воздушно-пылевым и
контактным путями. Ведущим путем передачи SARS-CoV-2 является воздушно-
капельный, который реализуется при кашле, чихании и разговоре на близком
(менее 2 метров) расстоянии. Контактный путь передачи реализуется во
время рукопожатий и других видах непосредственного контакта с
инфицированным человеком, а также через поверхности и предметы,
контаминированные вирусом.
По имеющимся научным данным возможен фекально-оральный механизм передачи
вируса. РНК SARS-CoV-2 обнаруживалась в образцах фекалий больных, как и
при других инфекциях, вызванных высокопатогенными коронавирусами.
Установлена роль COVID-19 как инфекции, связанной с оказанием
медицинской помощи. Медицинские работники подвергаются самому высокому
риску инфицирования, поскольку в процессе выполнения профессиональных
обязанностей имеют длительный аэрозольный контакт. Риск реализации
воздушно-капельного, пылевого и контактного путей передачи возбудителя
повышается в условиях несоблюдения требований
санитарно-противоэпидемического режима, правил эпидемиологической
безопасности, в том числе использования средств индивидуальной защиты.
Существует высокий риск формирования эпидемических очагов COVID-19
в организованных коллективах (воинские коллективы, образовательные
учреждения,
дома престарелых, психоневрологические диспансеры, общежития,
медицинские организации) при заносе инфекции, особенно в случае
нарушения санитарно- противоэпидемического режима. Также существует риск
возникновения множественных заболеваний в коллективах организаций
закрытого типа при несоблюдении мер профилактики инфекции.
Новая коронавирусная инфекция, вызванная SARS-CoV-2, включена в перечень
заболеваний, представляющих опасность для окружающих (постановление
Правительства Российской Федерации от 31 января 2020 г. № 66).
Стандартное определение случая заболевания COVID-19
Подозрительный на COVID-19 случай
Клинические проявления острой респираторной инфекции (ОРИ) (температура
(t) тела выше 37,5 °C и один или более из следующих признаков: кашель –
сухой или со скудной мокротой, одышка, ощущение заложенности в грудной
клетке, насыщение крови кислородом по данным пульсоксиметрии (SpO2) ≤
95%, боль в горле, заложенность носа или умеренная ринорея, нарушение
или потеря обоняния (гипосмия или аносмия), потеря вкуса (дисгевзия),
конъюнктивит, слабость, мышечные боли, головная боль, рвота, диарея,
кожная сыпь) при отсутствии других известных причин, которые объясняют
клиническую картину вне зависимости от эпидемиологического анамнеза.
Вероятный (клинически подтвержденный) случай COVID-19
кашель, сухой или со скудной мокротой, одышка, ощущение заложенности в
грудной клетке, SpO2 ≤ 95%, боль в горле, заложенность носа или
умеренная ринорея, нарушение или потеря обоняния (гипосмия или аносмия),
потеря вкуса (дисгевзия), конъюнктивит, слабость, мышечные боли,
головная боль, рвота, диарея, кожная сыпь) при наличии хотя бы одного из
эпидемиологических признаков:
- Возвращение из зарубежной поездки за 14 дней до появления симптомов;
- Наличие тесных контактов за последние 14 дней с лицом, находящимся под
наблюдением по COVID-19, который в последующем заболел; - Наличие тесных контактов за последние 14 дней с лицом, у которого
лабораторно подтвержден диагноз COVID-19; - Наличие профессиональных контактов с лицами, у которых выявлен
подозрительный или подтвержденный случай заболевания COVID-19.
Подтвержденный случай COVID-19
- Положительный результат лабораторного исследования на наличие РНК
SARS-CoV-2 с применением методов амплификации нуклеиновых кислот (МАНК)
или антигена SARS-CoV-2 c применением иммунохроматографического анализа
вне зависимости от клинических проявлений. - Положительный результат на антитела класса IgA, IgM и/или IgG у
пациентов с клинически подтвержденной инфекцией COVID-19.
КЛИНИЧЕСКИЕ ОСОБЕННОСТИ
Инкубационный период составляет от 2 до 14 суток, в среднем 5-7 суток. Для COVID-19 характерно наличие клинических симптомов ОРВИ:
- Повышение t тела (> 90%);
- Кашель (сухой или с небольшим количеством мокроты) в 80% случаев;
- Ощущение заложенности в грудной клетке (> 20%).
Также могут отмечаться боль в горле, насморк, снижение обоняния и вкуса,
признаки конъюнктивита.
Наиболее тяжелая одышка развивается к 6-8-му дню от момента заболевания. Также установлено, что среди первых симптомов могут быть миалгия (11%),
спутанность сознания (9%), головные боли (8%), кровохарканье (2-3%),
диарея (3%), тошнота, рвота, сердцебиение. Данные симптомы в начале
болезни могут наблюдаться и при отсутствии повышения температуры тела.
Клинические варианты и проявления COVID-19
- ОРВИ (поражение только верхних отделов дыхательных путей);
- Пневмония без дыхательной недостаточности;
- ОРДС (пневмония с ОДН);
- Сепсис, септический (инфекционно-токсический) шок;
- ДВС-синдром, тромбозы и тромбоэмболии.
Гипоксемия (SpO2 < 88%) развивается более чем у 30 % пациентов.
Классификация COVID-19 по степени тяжести
- Т тела < 38 °C, кашель, слабость, боли в горле
- Отсутствие критериев среднетяжелого и тяжелого течения
- Т тела > 38 °C
- ЧДД > 22/мин
- Одышка при физических нагрузках
- Изменения при КТ (рентгенографии), типичные для вирусного поражения
(объем поражения минимальный или средний; КТ 1-2) - SpO2 < 95%
- СРБ сыворотки крови >10 мг/л
- ЧДД > 30/мин
- SpO2 ≤ 93%
- PaO2 /FiO2 ≤ 300 мм рт.ст.
- Снижение уровня сознания, ажитация
- Нестабильная гемодинамика (систолическое АД менее 90 мм рт.ст. или
диастолическое АД менее 60 мм рт.ст., диурез менее 20 мл/час) - Изменения в легких при КТ (рентгенографии), типичные для вирусного
поражения (объем поражения значительный или субтотальный; КТ 3-4) - Лактат артериальной крови > 2 ммоль/л
- qSOFA > 2 балла
Крайне тяжелое течение
- Стойкая фебрильная лихорадка
- ОДН с необходимостью респираторной поддержки (инвазивная вентиляции
легких) - Изменения в легких при КТ (рентгенографии), типичные для вирусного
поражения критической степени (объем поражения значительный или
субтотальный; КТ 4) или картина ОРДС.
В среднем у 50% инфицированных заболевание протекает бессимптомно. У 80%
пациентов с наличием клинических симптомов заболевание протекает в
легкой форме ОРВИ.
Кожные сыпи при COVID-19
В настоящее время имеется ряд клинических наблюдений, описывающих кожные
сыпи при COVID-19, в связи с чем основной задачей клиницистов является
дифференциальная диагностика поражений кожи при COVID-19 от других
инфекционных экзантем, а также целого ряда дерматозов.
Анализ накапливающихся в литературе описаний клинических наблюдений
кожных сыпей у больных COVID-19, а также собственный опыт
продолжающегося динамического наблюдения наших соотечественников,
страдающих этим вирусным заболеванием, позволяет прийти к выводу о том,
что поражения кожи могут быть первыми признаками начала короновирусной
инфекции. Кроме того, многообразие наблюдаемых дерматозов и кожных сыпей
можно разделить на семь групп в зависимости от их этиологии и механизмов
развития:
1 группа — Ангииты кожи. Как правило, ангииты кожи имеют инфекционно-
аллергический генез и возникают на фоне инфекционных процессов
различной, в том числе вирусной этиологии. Классическим примером может
служить острая узловатая эритема на фоне обычной ОРВИ. При
короновирусной инфекции происходит поражение стенок мелких сосудов дермы
циркулирующими иммунными комплексами в виде депозитов с вирусными
антигенами. К особым формам, ассоциированным с COVID-19, можно отнести
акроваскулиты. Акральная приуроченность сыпи, возможно, обусловлена
сопутствующей заболеванию гипоксии.
2 группа — Папуло-сквамозные сыпи и розовый лишай. Представляют собой
характерные инфекционно-аллергические поражения кожи, также часто
ассоциированные с COVID-19. Клинической особенностью розового лишая при
короновирусной инфекции является отсутствие «материнской бляшки» (самого
крупного элемента, возникающего первым при классическом течении
дерматоза).
3 группа — Кореподобные сыпи и инфекционные эритемы. При COVID-19 эти
сыпи напоминают по своим клиническим характеристикам таковые,
характерные для кори или других вирусных инфекций и, тем самым,
указывают на патогенетическую близость к классическим вирусным
экзантемам.
4 группа — Папуло-везикулезные высыпания (по типу милиарии или эккринной потницы). Возникают на фоне субфебрилитета с многодневным повышенным
потоотделением у пациентов. В отличие от классической милиарии,
высыпания при COVID-19 характеризуются обширностью поражений кожных
покровов.
5 группа – Токсидермии. Напрямую не связаны с короновирусной инфекцией и
являются следствием индивидуальной непереносимости пациентами
определенных лекарственных препаратов.
6 группа – Крапивница. В зависимости от своего происхождения заболевание
может иметь двоякий характер. С одной стороны, уртикарные высыпания
могут быть предвестником начала COVID-19 или возникают вместе с ее
первыми симптомами. С другой стороны, крапивница нередко развивается
вследствие лекарственной непереносимости и в таком случае является
клинической формой токсидермии. Акральное расположение волдырей на фоне
COVID-19 также можно отнести к специфическим особенностям уртикарного
поражения кожи при этом вирусном заболевании.
7 группа – Артифициальные поражения (трофические изменения тканей лица). Являются следствием вынужденного длительного пребывания больных в прон-
позиции с целью улучшения дыхательной функции.
Особенности клинических проявлений у пациентов пожилого и старческого возраста
У пациентов старческого возраста может наблюдаться атипичная картина
заболевания без лихорадки и кашля вследствие сниженной реактивности. Симптомы COVID-19 могут быть невыраженными и не соответствовать тяжести
заболевания и серьезности прогноза. Атипичные симптомы COVID-19 у
пациентов пожилого и старческого возраста включают делирий и бред. Для
скрининга делирия рекомендуется использование краткой шкалы оценки
спутанности сознания (Таблица 1).
Таблица 1. Краткая шкала оценки спутанности сознания
* Ричмондская шкала ажитации (The Richmond Agitation-Sedation Scale, RASS)
+4 ВОИНСТВЕННЫЙ: воинственен, агрессивен, опасен для окружающих (срочно
сообщить врачу об этих явлениях)
+3 ОЧЕНЬ ВОЗБУЖДЕН: агрессивен, пытается вырвать трубки, капельницу или
катетер (сообщить врачу)
+2 ВОЗБУЖДЕН: частые бесцельные движения, сопротивление процедурам
+1 НЕСПОКОЕН: тревожен, неагрессивные движения
0 СПОКОЕН И ВНИМАТЕЛЕН
-1 СОНЛИВ: невнимателен, сонлив, но реагирует всегда на голос
-2 ЛЕГКАЯ СЕДАЦИЯ: просыпается на короткое время на голос
-3 СРЕДНЯЯ СЕДАЦИЯ: движение или открытие